
O Sistema HLA
Para o nosso organismo combater um patógeno, tem de ser capaz de o reconhecer ou – melhor dizendo – reconhecer pequenas moléculas que fazem parte deste mesmo patógeno, às quais chamamos de antigénios. Dispomos de várias células capazes de levar a cabo esta tarefa, mas falemos em específico dos linfócitos T.
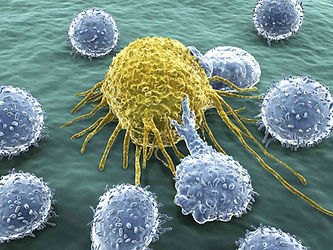
Reconhecimento de antigénios pelos linfócitos T
Estes linfócitos têm a capacidade de reconhecer moléculas estranhas na superfície de células do nosso organismo. Para estas moléculas (mais especificamente, proteínas) serem reconhecidas, têm de estar associadas a moléculas específicas, chamadas moléculas MHC (traduzindo do inglês, complexo major de histocompatibilidade), que funcionam como outdoors e são capazes de informar os linfócitos T sobre se há alguma infeção a decorrer ou até mesmo se a célula se está a tornar tumoral e deve ser eliminada. Existem dois tipos de moléculas MHC – os de classe I e os de classe II – que são reconhecidos por tipos distintos de linfócitos T.
O complexo HLA
A informação que codifica estas proteínas encontra-se no cromossoma 6 nos humanos, agrupada no complexo HLA, que compreende, em cada um de nós, vários genes. Podemos subdividir os genes deste complexo em várias subclasses:
-
HLA-A, HLA-B e HLA-C, que codificam MHC classe I, presente em praticamente todas as nossas células
-
HLA-DR, HLA-DP e HLA-DQ, que codificam MHC classe II, presente apenas nas células do sistema imunitário

Poligenia e polimorfismo
Cada tipo de molécula MHC consegue apresentar uma lista limitada de moléculas estranhas ao nosso organismo, de maneira que a elevada quantidade de genes permite aumentar o espetro de moléculas passíveis de ser apresentadas e, assim, melhorar a nossa defesa imunitária. Ao facto de estarem vários genes envolvidos na síntese destas moléculas MHC nós chamamos de poligenia. Além do mais, considera-se que este complexo é muito polimórfico, ou seja, na nossa população há múltiplas formas destes mesmos genes (a que nós chamamos de diferentes alelos) que diferem ligeiramente entre si e conferem vantagem de sobrevivência face a diferentes patógenos, não a nível individual, mas à população como um todo.
A cada um destes alelos foi dada uma nomenclatura, por exemplo HLA-A1, HLA-A2, e assim sucessivamente para cada um dos subtipos mencionados.
Em dezembro de 2016 já haviam sido identificados
3657
Alelos HLA-A
1977
Alelos HLA-DRB1
4459
Alelos HLA-B
978
Alelos HLA-DQB1
3290
Alelos HLA-C
716
Alelos HLA-DPB1
Hereditariedade do complexo HLA
Temos ainda que ter em conta que cada uma das nossas células tem dois cromossomas 6, um herdado do pai e outro herdado da mãe, daí que possamos ter, por exemplo proteínas HLA-A1, -B8, -Cw7, -DR3, -DQ2, e DPw1 de origem materna e proteínas HLA-A2, -B27, -Cw1, -DR4, -DQ3, e DPw4 de origem paterna. Dado haver uma variedade tão grande de diferentes alelos numa população, é muito raro que ambos os cromossomas tenham alelos iguais para estas proteínas, ou seja, geralmente, cada um dos cromossomas apresenta um alelo diferente para cada gene. A combinação de alelos presente num cromossoma pertencente ao complexo HLA chama-se de haplótipo MHC. Desta forma, uma vez que a maioria dos indivíduos têm dois haplótipos distintos, a descendência de um casal pode ter uma de quatro combinações possíveis de haplótipos. Consequentemente, há uma hipótese de 1 em 4 de dois irmãos partilharem exatamente os mesmos dois haplótipos dos progenitores, daí a dificuldade de, mesmo entre irmãos, ser difícil de encontrar um dador compatível para transplante.

MHC e rejeição de transplante
O polimorfismo HLA é benéfico para a sobrevivência da nossa espécie como um todo, mas torna muito provável o fenómeno de rejeição de um órgão transplantado, uma vez que o órgão do dador pode ser reconhecido como um corpo estranho ou como células infetadas por um vírus, se as moléculas MHC entre o dador e o recetor forem diferentes. Neste caso, os nossos linfócitos T vão atacar o órgão transplantado, sobretudo os seus vasos sanguíneos, levando à sua rejeição.
Mas se a função dos linfócitos T é de reconhecer as moléculas apresentadas pelo MHC, porque é que há esta reação? Ora, acontece que , na realidade, o linfócito T não reconhece a molécula estranha per se, mas sim reconhece o conjunto formado pela molécula estranha e pela molécula MHC. Portanto, é este facto que explica que haja uma reação de rejeição.
Basta a compatibilidade MHC para evitar a rejeição?
É importante notar que mesmo uma compatibilidade perfeita de alelos HLA entre dador e recetor não garante que não se vá desenvolver uma reação de rejeição, ainda que menos severa. Tal acontece porque, logicamente, as moléculas MHC não são as únicas que diferem entre dois indivíduos diferentes, apesar de serem as principais intervenientes em processos de rejeição. Cada um de nós têm uma sequência de DNA única, de maneira que será percetível que também outras das nossas proteínas serão ligeiramente diferentes entre cada um de nós. São estas proteínas que determinam o desenvolvimento de processos de rejeição, ainda que menos agudos e mais prolongados, mas que eventualmente justificam o facto de um órgão transplantado ser efémero.
Na realidade, a resposta a estas moléculas que não MHC é muito semelhante ao que se processa aquando de uma infeção viral: há reconhecimento de células diferentes e eliminação das mesmas. A diferença é que, enquanto numa infeção viral se destrói apenas as células infetadas, num transplante todas as células do órgão em causa ficarão comprometidas, visto que todas têm as moléculas estranhas.
Por esta mesma razão, mesmo quando há uma boa compatibilidade HLA, deve apostar-se na imunossupressão, para melhorar a durabilidade do transplante.
